В допълнение към технологиите, синтезът на гликозиди винаги е бил от интерес за науката, тъй като е много често срещана реакция в природата. Последните статии на Шмит и Тошима и Тацута, както и многобройните цитирани там източници, коментират широк спектър от синтетични потенциали.
При синтеза на гликозиди, многозахарните компоненти се комбинират с нуклеофили, като алкохоли, въглехидрати или протеини. Ако е необходима селективна реакция с една от хидроксилните групи на въглехидрата, всички останали функции трябва да бъдат защитени в първия етап. По принцип, ензимните или микробните процеси, поради тяхната селективност, могат да заместят сложните етапи на химическа защита и премахване на защитни групи, за да селективно отделят гликозиди в определени региони. Въпреки това, поради дългата история на алкилните гликозиди, приложението на ензими в синтеза на гликозиди не е широко проучено и приложено.
Поради капацитета на подходящите ензимни системи и високите производствени разходи, ензимният синтез на алкилполигликозиди не е готов за надграждане до индустриално ниво и се предпочитат химичните методи.
През 1870 г. М.А. Коли съобщава за синтеза на „ацетохлорхидроза“ (1, фигура 2) чрез реакция на декстроза (глюкоза) с ацетилхлорид, което в крайна сметка води до историята на пътищата за синтез на гликозиди.
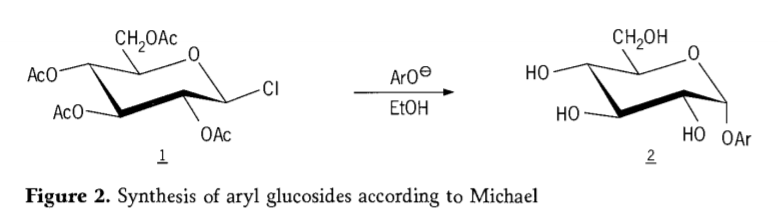
Тетра-0-ацетил-глюкопиранозил халиди (ацетохалоглукози) по-късно се оказват полезни междинни продукти за стереоселективния синтез на чисти алкил глюкозиди. През 1879 г. Артър Майкъл успява да получи определени, кристализиращи се арил гликозиди от междинните продукти и фенолатите на Коли (Аро-, Фигура 2).
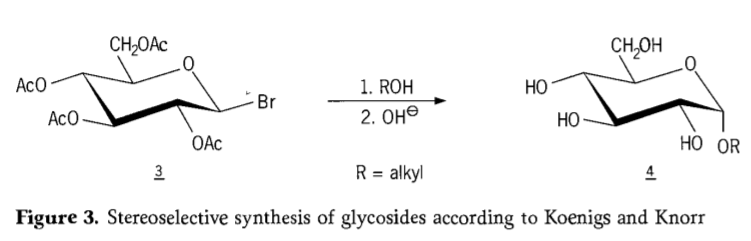
През 1901 г., синтезът на Майкъл до широк спектър от въглехидрати и хидроксилни агликони, когато В. Кьонигс и Е. Кнор представят своя подобрен стереоселективен процес на гликозидиране (Фигура 3). Реакцията включва SN2 заместване при аномерния въглерод и протича стереоселективно с инверсия на конфигурацията, произвеждайки например α-глюкозид 4 от β-аномера на ацеобромоглюкозния междинен продукт 3. Синтезът на Кьонигс-Кнор протича в присъствието на сребърни или живачни промотори.
През 1893 г. Емил Фишер предлага фундаментално различен подход към синтеза на алкил глюкозиди. Този процес е добре известен като „фишерова гликозидация“ и представлява киселинно катализирана реакция на гликози с алкохоли. Въпреки това, всеки исторически преглед трябва да включва и първия докладван опит на А. Готие през 1874 г. да превърне декстроза с безводен етанол в присъствието на солна киселина. Поради подвеждащ елементен анализ, Готие смята, че е получил „диглюкоза“. По-късно Фишер демонстрира, че „диглюкозата“ на Готие всъщност е главно етил глюкозид (Фигура 4).
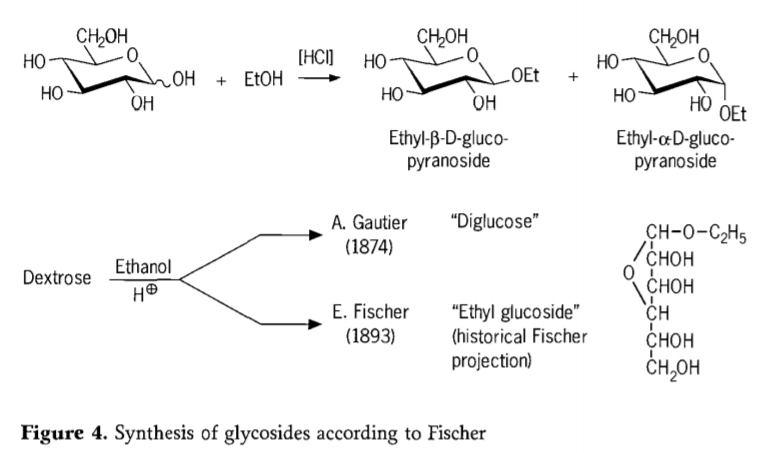
Фишер правилно дефинира структурата на етилглюкозида, както може да се види от предложената историческа фуранозидна формула. Всъщност, продуктите на гликозидирането на Фишер са сложни, предимно равновесни смеси от α/β-аномери и пиранозидни/фуранозидни изомери, които също така съдържат произволно свързани гликозидни олигомери.
Съответно, отделните молекулни видове не са лесни за изолиране от реакционните смеси на Фишер, което е било сериозен проблем в миналото. След известно усъвършенстване на този метод на синтез, Фишер впоследствие възприема синтеза на Кьонигс-Кнор за своите изследвания. Използвайки този процес, Е. Фишер и Б. Хелферих са първите, които съобщават за синтеза на дълговерижен алкил глюкозид, проявяващ повърхностноактивни свойства през 1911 г.
Още през 1893 г. Фишер правилно е забелязал съществени свойства на алкилните гликозиди, като например тяхната висока стабилност към окисление и хидролиза, особено в силно алкална среда. И двете характеристики са ценни за алкилните полигликозиди в приложенията им като повърхностноактивни вещества.
Изследванията, свързани с реакцията на гликозидиране, все още продължават и напоследък са разработени няколко интересни пътя за получаване на гликозиди. Някои от процедурите за синтез на гликозиди са обобщени на Фигура 5.
Като цяло, процесите на химично гликозидиране могат да бъдат разделени на процеси, водещи до сложни олигомерни равновесия в киселинно-катализиран гликозилен обмен.
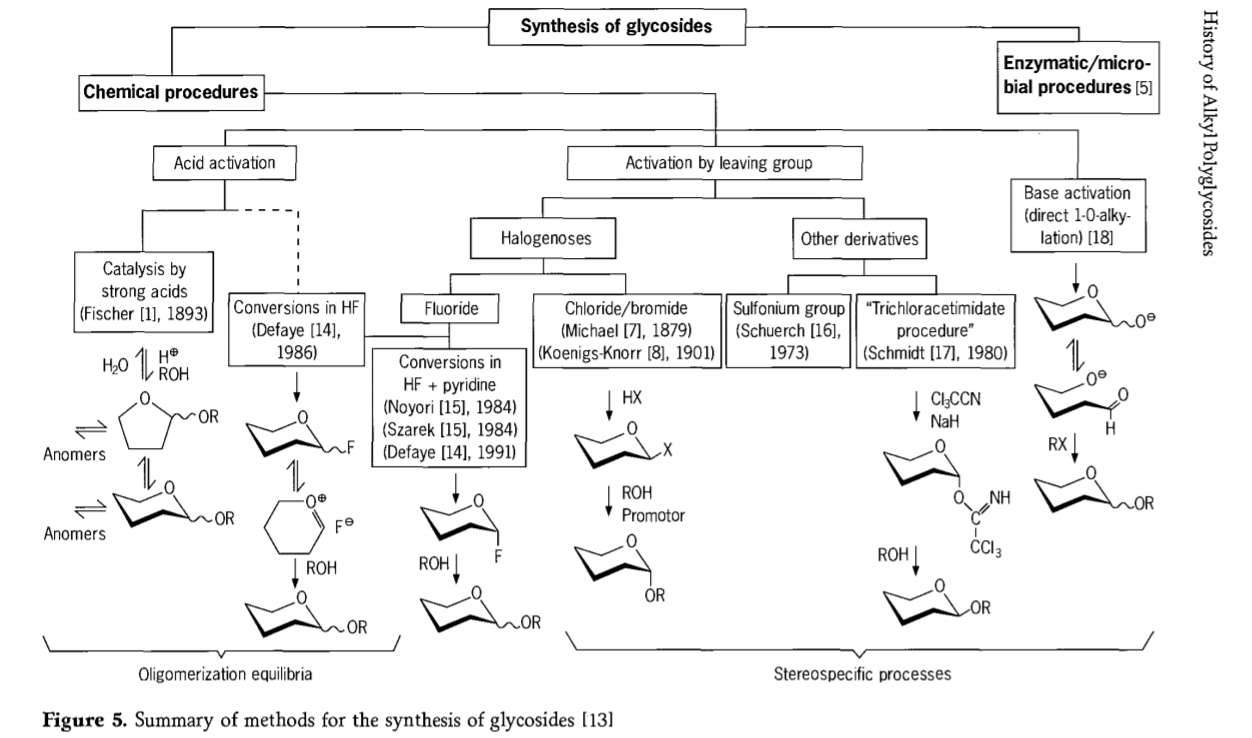
Реакции върху подходящо активирани въглехидратни субстрати (гликозидни реакции на Фишер и реакции на флуороводород (HF) с незащитени въглехидратни молекули) и кинетично контролирани, необратими и главно стереотаксични заместителни реакции. Вторият тип процедура може да доведе до образуването на отделни видове, а не до сложни смеси от реакции, особено когато се комбинира с техники за консервативни групи. Въглехидратите могат да оставят групи върху ектопичния въглерод, като халогенни атоми, сулфонили или трихлороацетимидатни групи, или да бъдат активирани от бази преди превръщането им в трифлатни естери.
В конкретния случай на гликозидации във флуороводород или в смеси от флуороводород и пиридин (пиридиниев поли[флуороводород]), гликозилфлуоридите се образуват in situ и плавно се превръщат в гликозиди, например с алкохоли. Флуороводородът е показан като силно активираща, неразграждаща се реакционна среда; наблюдава се равновесна автокондензация (олигомеризация), подобно на процеса на Фишер, въпреки че реакционният механизъм вероятно е различен.
Химически чистите алкил гликозиди са подходящи само за много специални приложения. Например, алкил гликозидите са използвани успешно в биохимични изследвания за кристализация на мембранни протеини, като например триизмерната кристализация на порин и бактериородопсин в присъствието на октил β-D-глюкопиранозид (по-нататъшни експерименти, базирани на тази работа, водят до Нобелова награда за химия за Дайзенхофер, Хубер и Мишел през 1988 г.).
В хода на разработването на алкилполигликозиди, стереоселективни методи са били използвани в лабораторен мащаб за синтезиране на различни моделни вещества и за изучаване на техните физикохимични свойства. Поради тяхната сложност, нестабилност на междинните продукти и количеството и критичния характер на отпадъчните продукти от процеса, синтезите от типа на Кьонигс-Кнор и други техники със защитни групи биха създали значителни технически и икономически проблеми. Процесите от типа на Фишер са сравнително по-малко сложни и по-лесни за изпълнение в търговски мащаб и съответно са предпочитаният метод за производство на алкилполигликозиди в голям мащаб.
Време на публикуване: 12 септември 2020 г.





